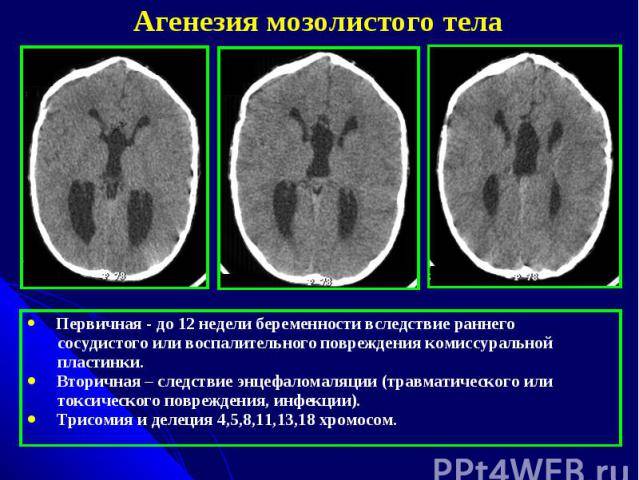
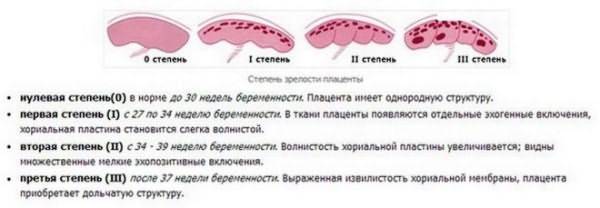
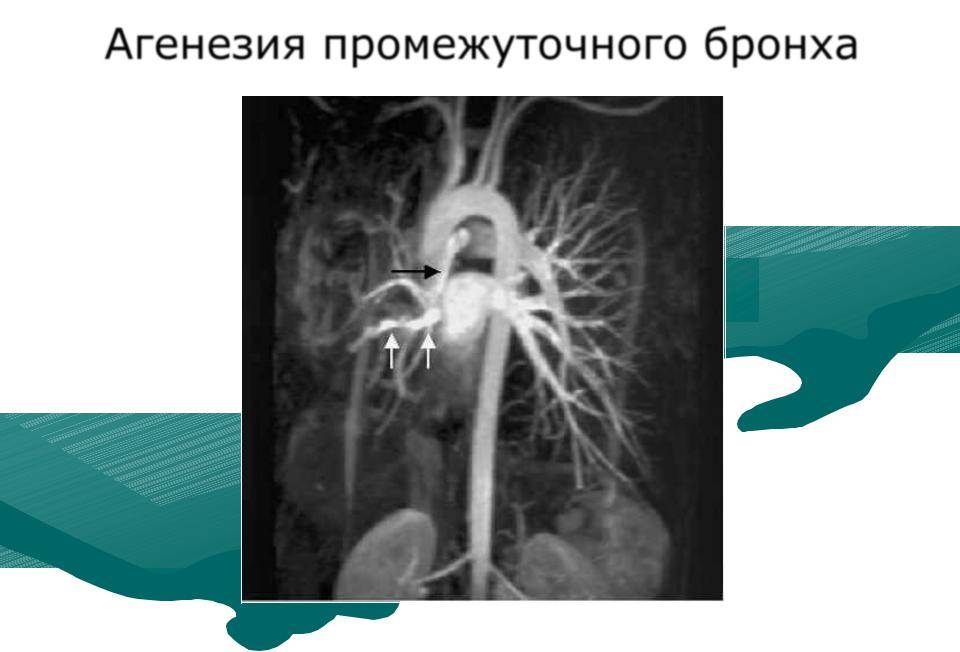
Когда следует обратиться к генетику?
Во избежание серьезных проблем о здоровье ребенка необходимо позаботиться задолго до его зачатия. Планируя беременность, осмотр и консультация профессионала не помешают, если в семье были случаи появления на свет детей с хромосомными или генетическими болезнями, а также врожденными дефектами развития. Незаменим визит к врачу при возрасте жены меньше 18 или больше 35 лет, для мужа критической планкой считается возраст после 45 лет. Показателем для посещения генетика является родственная связь между супругами, умственная отсталость жены, прием медикаментов, алкоголя и наркотиков перед зачатием, наличие вредных условий труда, тяжелая болезнь хотя бы одного из супругов в этот период и прохождение рентгеновского исследования.
В течение беременности не стоит откладывать визит, если у женщины диагностировано венерическое заболевание или вирусная инфекция, а также отмечены случаи мертворождения в прошлом. В группе риска находятся беременные, которые прошли рентгеновское обследование, принимали медикаменты без медицинской консультации или контактировали с больным краснухой.
Врач поможет выявить возможные патологии, если один из супругов страдает задержкой полового, речевого, физического или умственного развития. При этом наличие пороков может быть как единичным, так и множественным
Особое внимание уделяется пациентам с нарушениями слуха и зрения, ожирением различной степени, преждевременным половым созреванием в анамнезе и бесплодием сроком свыше двух лет. К негативным факторам относится полное отсутствие менструаций или нарушенный цикл, нестандартное строение тела, наличие хронических заболеваний, не поддающихся лечению, и самопроизвольные выкидыши
Врожденными заболеваниями занимаются врачи соответствующего профиля, у которых ребенок в обязательном порядке наблюдается после рождения.
Патологии плода, вызванные алкогольной зависимостью беременной
Самая распространённая патология, вызванная употреблением алкоголя беременной женщиной, — синдром Миллера-Дикера. Мутация происходит в гене 17-й хромосомы. Главная причина аномалии — интоксикация плода альдегидами, передающимися через материнскую кровь.
На УЗИ синдром Миллера-Дикера выражается в многоводии, отставании внутриутробного развития плода и снижении его двигательной активности. На более поздних сроках можно увидеть утолщение коры головного мозга при разглаживании мозговых извилин.
Голова у больных детей меньше положенного размера, лоб выпуклый, плоский затылок, челюсть недоразвита (алкогольная дизморфия). Ушные раковины расположены ниже положенного уровня, пальцы неправильной формы, тазобедренные суставы находятся на зачаточном уровне, стопы укорочены, задний проход сросшийся.
Такие дети обычно умирают в возрасте в 2 лет из-за аспирационной пневмонии. У них глубокая умственная отсталость и отсутствуют даже обычные рефлексы (глотание, моргание).
Диагностика врожденной патологии
В наше время, благодаря достижениям современной медицины, возможна ранняя диагностика врожденной патологии во внутриутробном периоде. Информация, полученная после диагностики врожденных пороков, необходима для принятия решения о дальнейшей тактике ведения пациентки:
- срочного лечения врожденного порока;
- проведения родов в специализированных учреждениях для своевременного лечения врожденных пороков;
- прерывание беременности при невозможности лечения врожденного порока и нарушениях, несовместимых с жизнью.
Стоит отметить, что терапия детской врожденной патологии различается по степени тяжести и природе порока. По данным статистики, врожденные патологии плода в 25% случаев приводят к гибели малыша в течение 1 года жизни. В 25% врожденные пороки развития у детей приводят к умственным и физическим отклонениям. И только в 5% случаев есть возможность проведения лечения детской врожденной патологии.
Диагностика врожденной патологии заключается в проведении прямых (инвазивных и неинвазивных) и непрямых способов исследования.
Непрямые методы диагностики врожденных пороков: анализы крови на АФП, ХГЧ, гормоны, иммунологические, серологические, генетические тесты и т.п. На основании результатов этих исследований можно предположить наличие или высокий риск развития врожденных пороков плода. Особое значение в диагностике врожденной патологии имеет определение уровня АФП и ХГЧ, так как отклонения от нормы часто предполагают формирование врожденной патологии плода, в частности нервной системы.
Помимо этих способов исследования, все беременные проходят неинвазивные прямые методы диагностики врожденных пороков в плановом порядке: УЗИ, допплерометрия, КТГ. УЗИ проводится 3 раза в течение всего срока беременности, но при необходимости назначают дополнительные процедуры. Так как к 19-20 неделе уже сформированы практически все органы и системы, то видны на УЗИ врожденные пороки развития плода в 80-86% случаев. Одна из разновидностей УЗИ – допплерометрия, позволяющая оценить параметры кровообращения. При этом признаки врожденных пороков развития на УЗИ определяются в ранние сроки беременности.
На 28-30 неделе беременности и во время родов беременным проводят КТГ, этот метод позволяет оценить характер сердечных сокращений плода (при помощи УЗ датчика) и схваток, а также определить вероятность осложнений родового и послеродового периода. Стоит отметить, что КТГ позволяет определить УЗ признаки врожденных пороков развития сердца и системы кровообращения, а также врожденные пороки центральной нервной системы. Если результаты неинвазивной диагностики врожденных пороков плода неудовлетворительны, то прибегают к дополнительным инвазивным методикам для изучения генетического материала плода (амниоцентезу, плацентоцентезу, хорионцентезу, забору крови пуповины, биопсии ворсин хориона).
Лечение
Для выбора оптимального метода лечения необходимо записаться на приём к торакальному хирургу или к пульмонологу. Характер терапии определяется общим состоянием пациента, степенью проявления патологии, прогнозами на лечение. Немедленное хирургическое вмешательство требуется в следующих случаях выраженной дыхательной недостаточности:
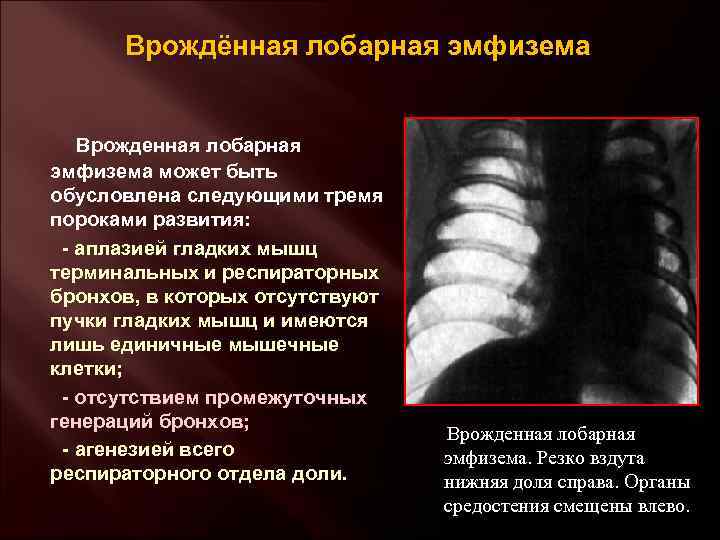
- Лобарная эмфизема;
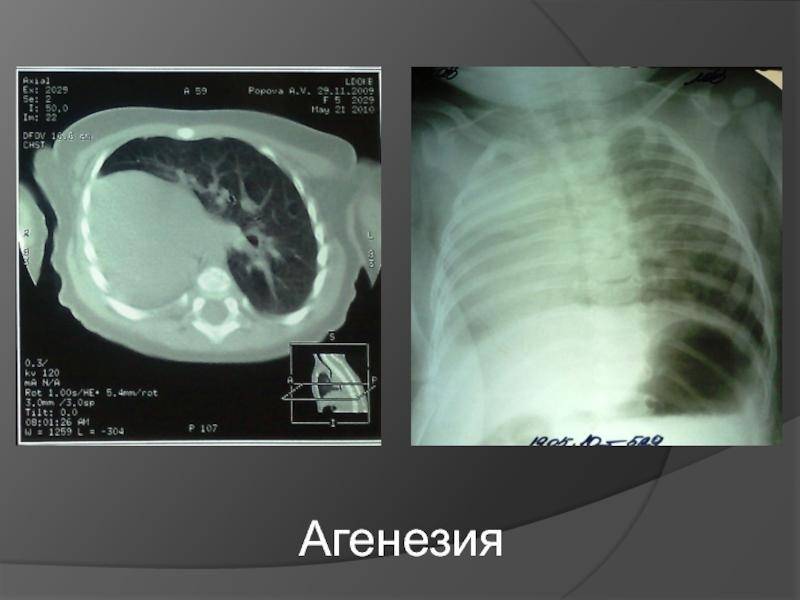
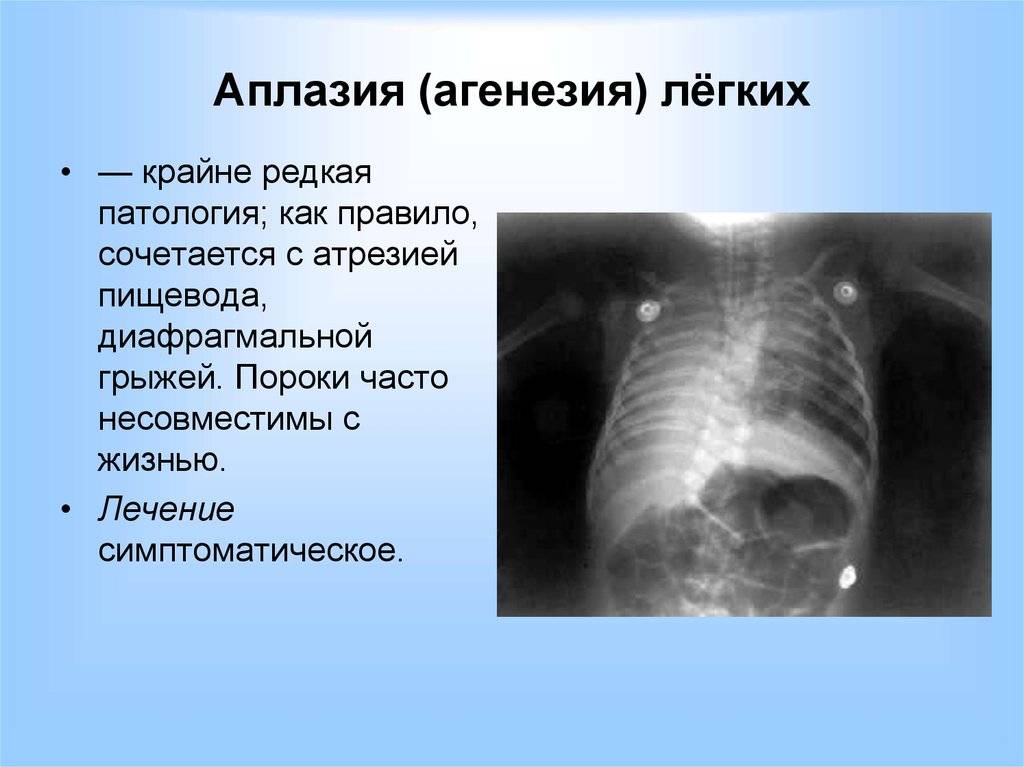
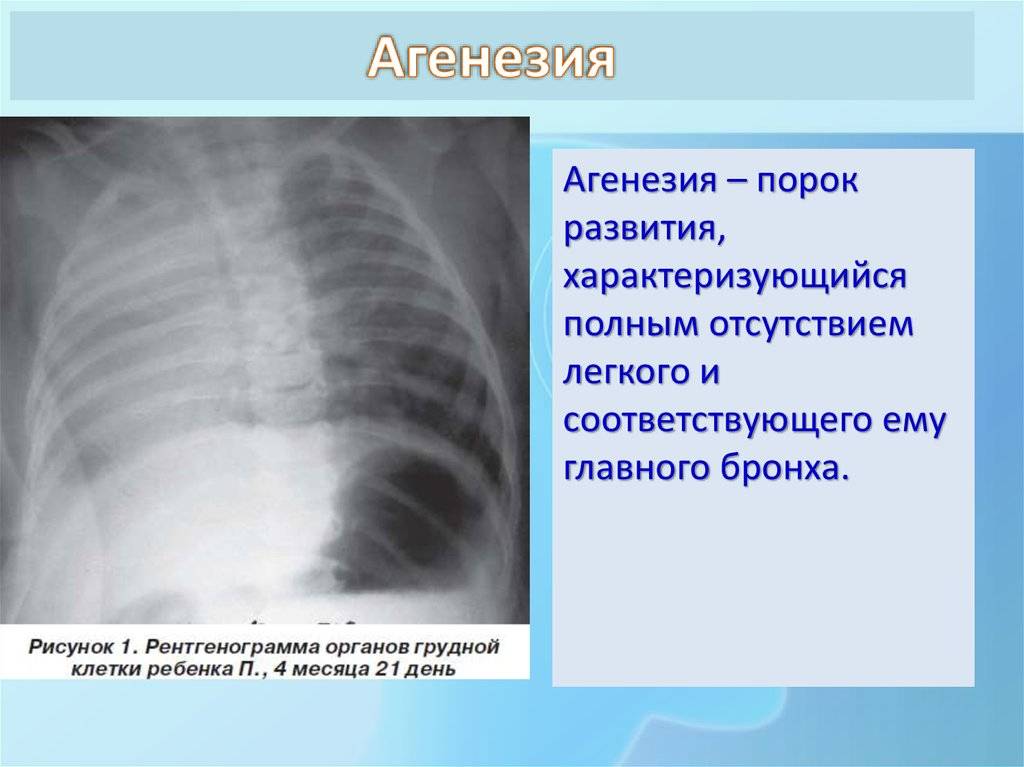
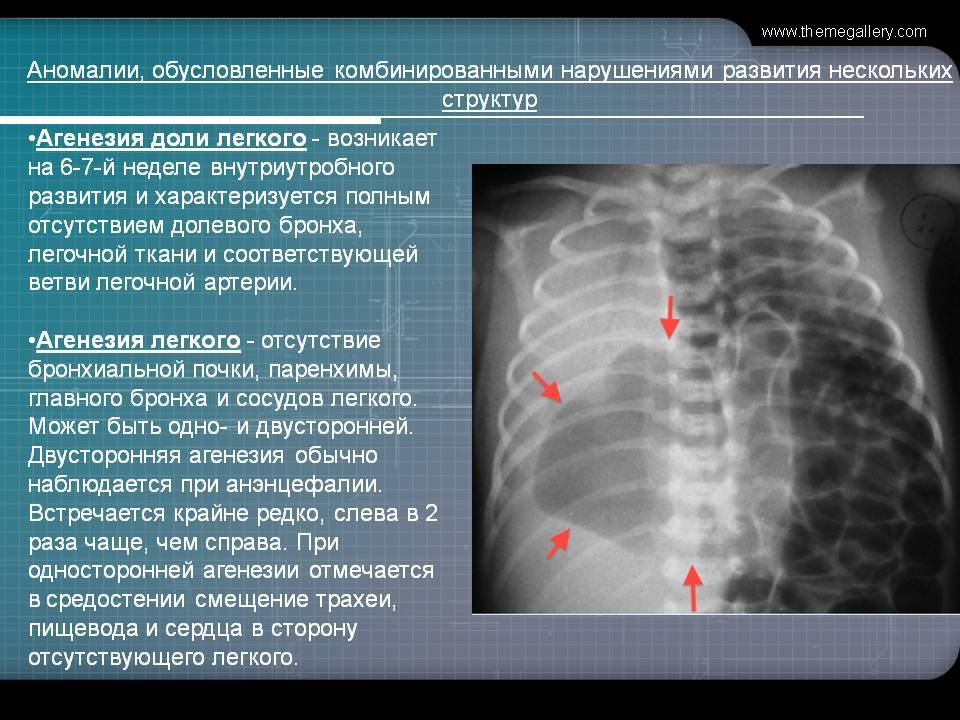
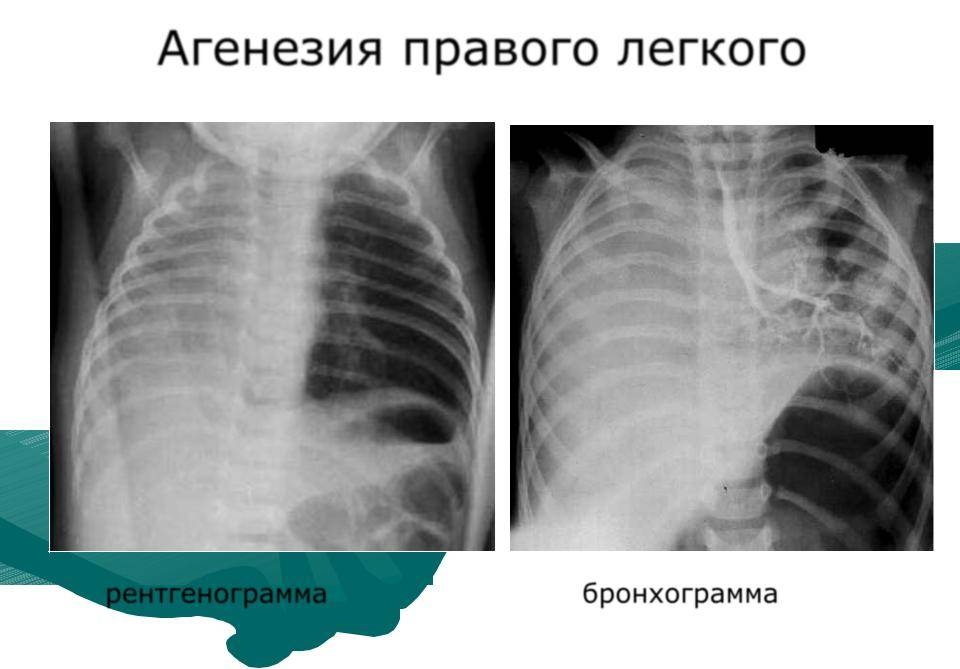
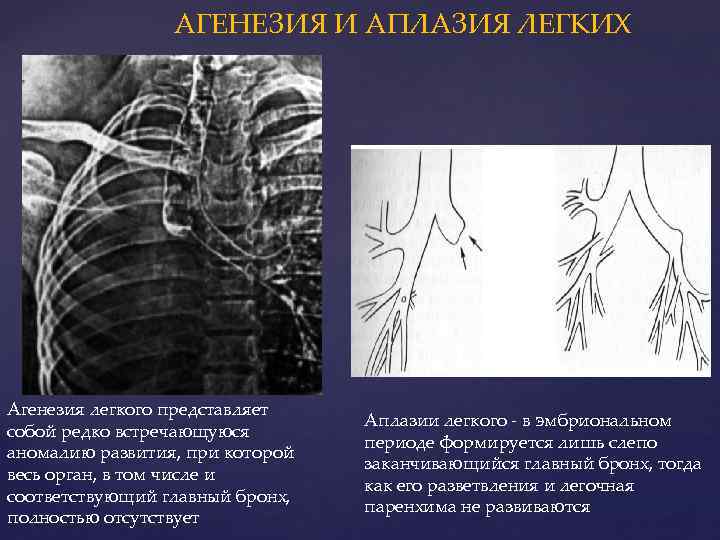
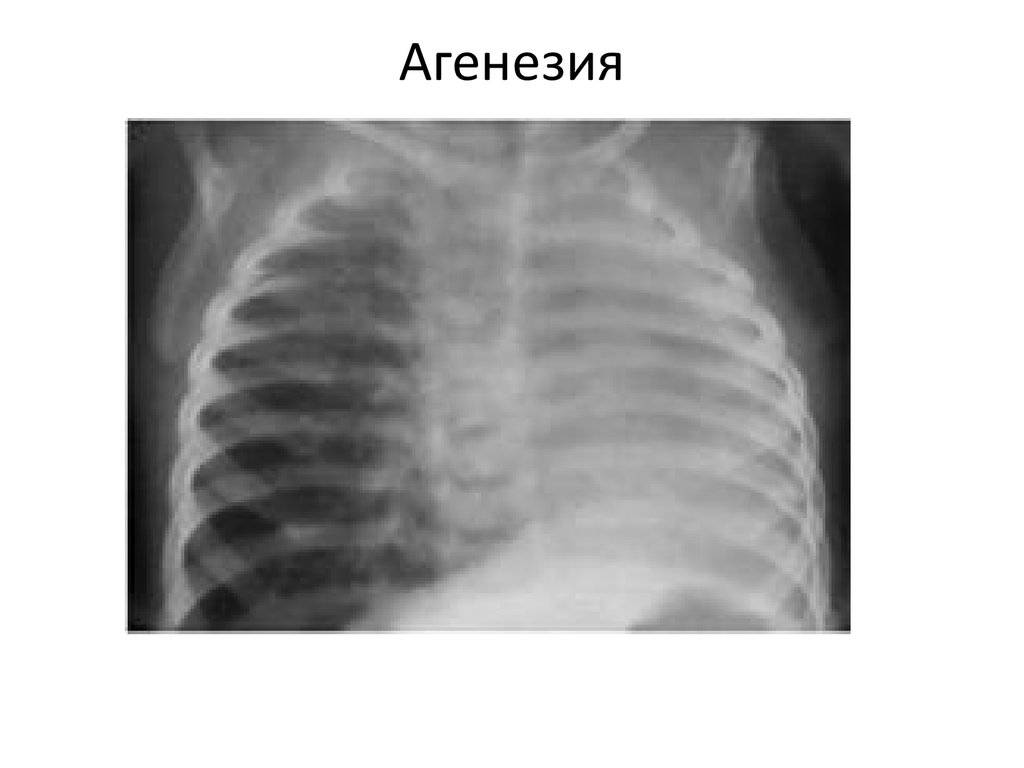
- Агенезия лёгких;
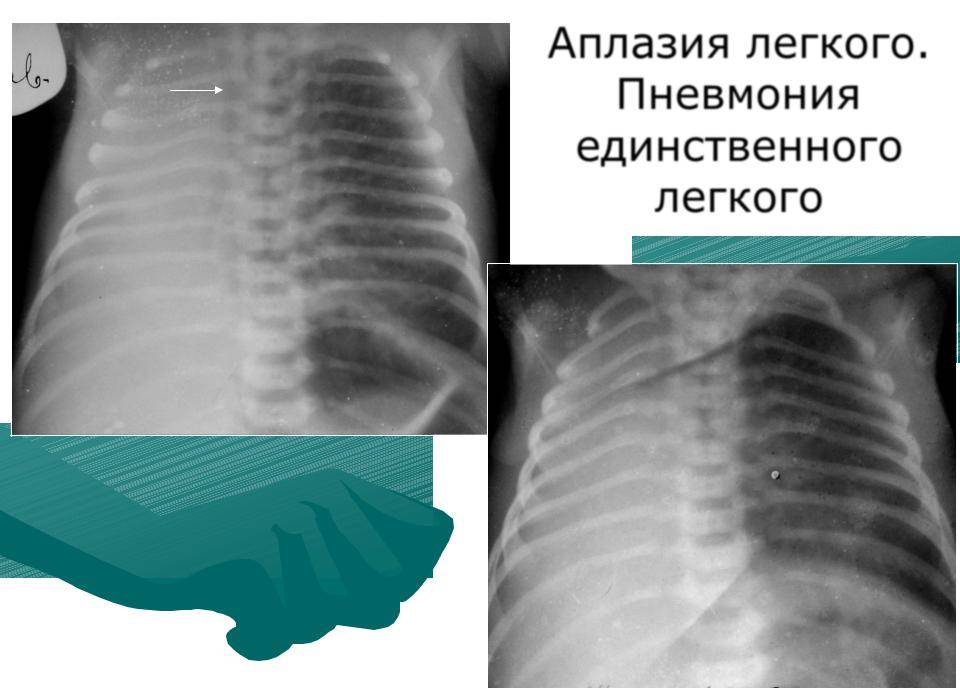
- Аплазия;
- Стеноз бронхов или трахеи;
- Трахеопищеводный свищ.
Наиболее распространённая методика лечения бронхоэктазов – удаление изменённой области органа, однако возможно и медикаментозное лечение, что зависит от количества рецидивов и объёма изменённой лёгочной ткани.
Также важно проведение консервативного лечения, которое позволяет предупредить развитие гнойных процессов: массаж грудной клетки, бронхоальвеолярный лаваж, ЛФК, ингаляции и др
ДЫХАТЕЛЬНЫЕ РАССТРОЙСТВА У НОВОРОЖДЕННЫХ
Синдром дыхательных расстройств новорожденного проявляется в первую очередь дыхательной недостаточностью.
Наиболее
часто синдром дыхательных расстройств наблюдается у недоношенных детей,
что связано с незрелостью системы сурфактанта (созревание системы
сурфактанта завершается к 35-36 нед) и его дефицитом к моменту рождения.
Недостаток сурфактанта – поверхностно активного вещества,
синтезируемого альвеолоцитами 2-го типа, – приводит к спадению альвеол
на выдохе и в результате, к снижению площади газообмена в легких,
гипо-ксемии и гиперкапнии. Незрелость системы сурфактанта приводит к
развитию гиалиновых мембран, отечно-геморрагического синдрома и др.
Гипоксия
плода как патогенетический фактор синдрома дыхательных расстройств
имеет не меньшее значение, чем гестационный возраст к моменту рождения.
Гипоксия может приводить к вазоконстрикции и гипоперфузии легких,
инактивации альвеолярного сурфактанта.
Одной из причин
синдрома дыхательных расстройств является аспирация околоплодных вод,
мекония и крови, которые вызывают обструкцию дыхательных путей и
повреждают сурфактантную систему легких, в результате чего у
новорожденных развивается дыхательная недостаточность.
Развитию
синдрома дыхательных расстройств способствуют задержка резорбции
фетальной жидкости из дыхательных путей новорожденных, персистирующие
фетальные коммуникации, а также пневмония.
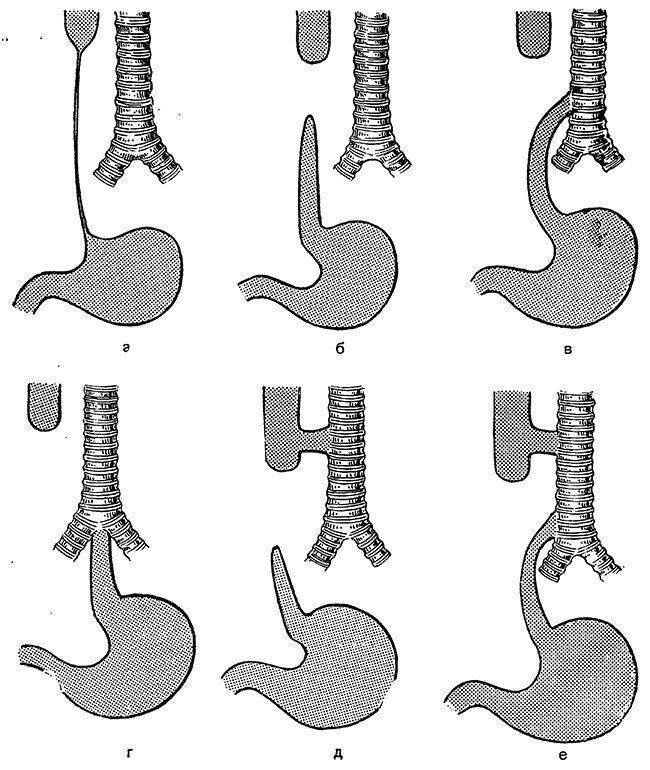
Острое
развитие дыхательной недостаточности в первые часы и дни после рождения
может быть обусловлено пороками развития верхних дыхательных путей и
легких (атрезия хоан, пищеводно-трахеальные свищи, долевая эмфизема,
агенезия и гипоплазия легких, поликистоз, диафрагмальная грыжа).
СИНДРОМ ВНЕЗАПНОЙ СМЕРТИ МЛАДЕНЦЕВ
Синдром
внезапной смерти младенцев – внезапная гибель ребёнка моложе
1 года в случае, когда причины гибели неясны даже после тщательного
посмертного исследования. Больной ребёнок может умереть внезапно при
отсутствии клинически выраженных признаков заболевания.
Возможные причинывнезапной
смерти: инфекционные болезни, врождённые пороки сердца, нарушения
сердечной проводимости, врождённые и приобретённые нарушения ЦНС с
судорогами и приступами апноэ, опухоли мозга, заболевания и состояния,
протекающие с гипогликемией, механическая асфиксия, отравления, травмы.
Если при патологоанатомическом исследовании или сборе анамнеза выявляют
признаки перечисленных заболеваний и состояний, то такие случаи не
относят к синдрому внезапной смерти ребёнка.
Частота
синдрома внезапной смерти составляет 1-5 случаев на
1000 живорождённых. В настоящее время частота имеет тенденцию к
росту, так как очень высокий риск развития синдрома внезапной смерти
отмечают у глубоко недоношенных детей, число их растёт в связи с
успехами выхаживания. Пик частоты синдрома – период 2-6 мес.
Выделяют факторы риска со стороны матери и плода.
•
Факторы риска со стороны матери: возраст моложе 20 лет,
низкое социально-экономическое положение, короткий промежуток между
беременностями, многоплодная беременность, курение, приём наркотиков и
алкоголя, инфекции мочевых путей во время беременности.
•
Факторы риска со стороны плода: недоношенность, низкая масса тела
при рождении, мужской пол, внутриутробная гипоксия, нарушение
терморегуляции (гипо- и гипертермия), предшествующие приступы апноэ,
перенесённая незадолго до смерти респираторная инфекция.
Этиология и патогенез
Единой точки зрения на этиологию и патогенез синдрома внезапной смерти
не существует. Наиболее распространена теория апноэ, согласно ей
остановка дыхания – основной механизм наступления смерти. Апноэ
центрального генеза связывают с незрелостью дыхательных центров
новорождённого, его повышенной чувствительностью к гипоксии,
гиперкапнии, изменению температуры тела и другим факторам. Кроме того,
установлено, что у детей до 6 мес затруднено переключение носового
дыхания на ротовое, особенно во время сна. Поэтому при отёке или
гиперсекреции слизи в носоглотке может возникнуть механическая
обструкция дыхательных путей.
ИЗОСЕРОЛОГИЧЕСКАЯ НЕСОВМЕСТИМОСТЬ КРОВИ МАТЕРИ И ПЛОДА. ГЕМОЛИТИЧЕСКАЯ БОЛЕЗНЬ ПЛОДА И НОВОРОЖДЕННОГО
Причиной
изосерологической несовместимости крови матери и плода является
различие антигенных факторов эритроцитов по системе резус: кровь матери
резус-отрицательная, плода – резус-положительная. Выявление у женщин с
резус-отрицательной кровью антирезус-антител указывает на сенсибилизацию
к резус-фактору, вследствие которой возможно развитие гемолитической
болезни плода и новорожденного (синоним – эритробластоз).
Резус-фактор
– система аллогенных эритроцитарных антигенов человека, дифференциация
которого начинается в ранние сроки внутриутробного развития (с 6-8 нед
гестации).
Белковый фактор в эритроцитах, обладающий
антигенными свойствами, был впервые обнаружен американскими учеными К.
Ландштейнером и А. Винером в 1940 г. В эксперименте они показали, что
эритроциты обезьян (макака-резус), введенные кроликам, вызывали у
кроликов выработку антител.
В настоящее время
выделяют 6 основных резус-антигенов Rh (Dd, Cc, Ee). Каждый генный
комплекс состоит из трех антигенных детерминант: D или отсутствие D, С
или с, Е или е в различных комбинациях. Существование антигена d не
подтверждено, так как не известен ген, отвечающий за синтез этого
антигена. Несмотря на это, символ d применяется в иммуногематологии для
обозначения отсутствия антигена D на эритроцитах при описании фенотипов.
Другими изосерологическими системами крови, с
которыми может быть связан иммунный конфликт, являются системы
Келл-Челлано, Даффи, Кидд, MNSs, Лютеран.
ГНОЙНО-СЕПТИЧЕСКИЕ ЗАБОЛЕВАНИЯ НОВОРОЖДЕННЫХ
Анатомо-физиологические
особенности, сниженная иммунная реактивность обусловливают высокую
восприимчивость новорожденных к гнойно-воспалительным инфекциям.
Инфицирование может наступить как во внутриутробном периоде, так и сразу
после рождения.
У новорожденных грань между
локальными и генерализованными формами гнойной инфекции в значительной
мере условна, так как возможен быстрый переход местного воспалительного
процесса в генерализованную инфекцию.
Клокальным формам относятся гнойно-воспалительные заболевания кожи и слизистых оболочек.
Кожа
новорожденных подвергается инфицированию наиболее часто. Различные
клинические формы поражения при этом объединяют под названием пиодермии.
Пиодермии развиваются под воздействием гноеродных микроорганизмов
(стафилококки, стрептококки, гонококки, протей, кишечная палочка,
синегнойная палочка и др.).
Везикулопустулез – поверхностная
стафилодермия новорожденных – встречается наиболее часто. Процесс
локализуется в устьях экзокринных потовых желез. Возникновению
заболевания могут способствовать перегревание, повышенная потливость,
мацерация. Фолликулярные пустулы размером с просяное зерно или горошину
располагаются по всему кожному покрову, чаще локализуются на спине, в
складках, на коже шеи, груди, в области ягодиц и на волосистой части
головы. Лечение местное (бриллиантовая зелень, метилвиолет, 2% раствор
перманганата калия). Антибактериальная терапия, как правило, не
проводится.
Псевдофурункулез – заболевание
мерокринных потовых желез у детей грудного возраста (множественные
абсцессы потовых желез, псевдофурункулез Фингера). Развитию заболевания
способствуют недоношенность, иммунодефицитные состояния, искусственное
вскармливание, дефекты ухода, повышенная потливость. Высыпания чаще
всего располагаются на затылке, спине, ягодицах, бедрах, возможно
распространение на кожу груди и живота. Заболевание сопровождается
нарушением общего состояния с повышением температуры тела. Местное
лечение осуществляют 2% спиртовыми или водными растворами анилиновых
красителей, присыпками из окиси цинка (10 %) с тальком. По показаниям
назначают антибиотики (с учетом данных антибиотикограммы) и
иммунозаместительную терапию.
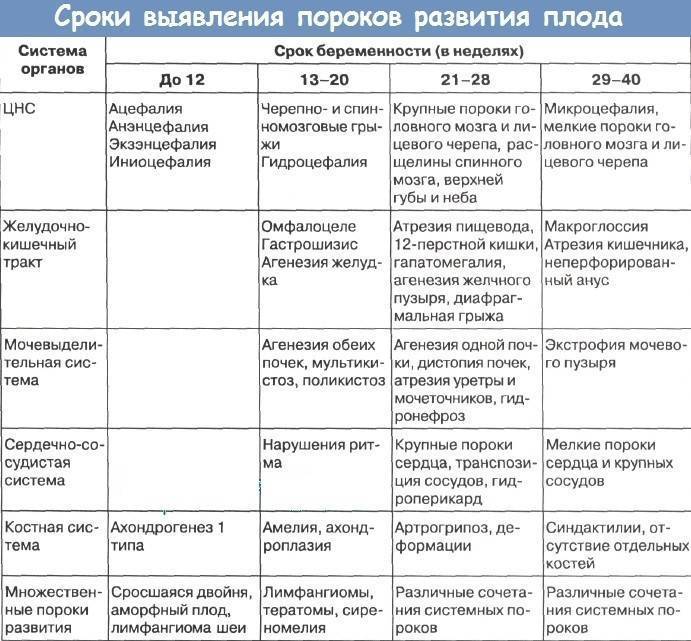
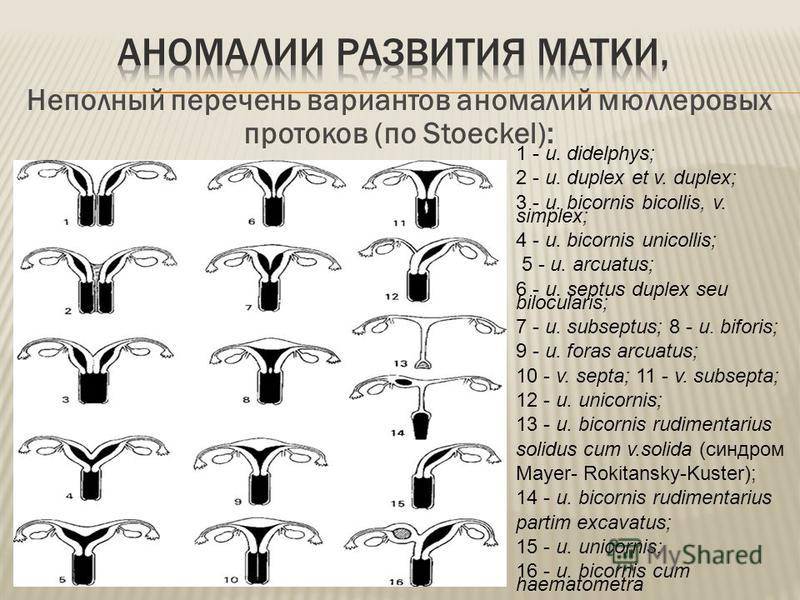
Аномалии развития плода: классификация
К данной категории принадлежат следующие заболевания:
Аномалии развития нервной трубки. Самой распространенной патологией ЦНС плода является анэнцефалия – врожденное отсутствие свода черепа и больших полушарий головного мозга. На УЗИ диагностируется на сроке 11-12 недель. Гидроцефалия обнаруживается на 18-й неделе беременности – по расширению передних и задних рогов боковых желудочков. Патологическое уменьшение головки плода (микроцефалия) возникает, как правило, на фоне других смежных заболеваний, и очень редко – в чистом виде. В таких случаях врач проводит УЗИ с разницей в несколько недель (для получения максимально достоверной картины). Округлое выпячивание в области костей свода черепа (энцефаломенингоцеле) диагностируют чаще всего на затылке, и подобная патология также требует повторного УЗИ.
Отклонения в развитии позвоночника наблюдаются в основном в поясничном и шейном отделе. Увидеть позвоночник на УЗИ можно с 15-й недели беременности, примерно с 18-й недели диагностируются (при наличии) пороки его строения. Самым страшным является кистозная гигрома, поражающая лимфатическую систему. На УЗИ при таком диагнозе видно кисту в шейном отделе позвоночника. Если данное заболевание сопряжено с другими патологиями лимфатической системы, плод гибнет. Сложно выявить миеломенингоцеле (образование состоит из жидкости и элементов спинного мозга) и расщепление позвоночника – эти патологии требуют применения аппаратуры экспертного класса.
Среди патологий развития органов ЖКТ чаще всего выявляют атрезию двенадцатиперстной кишки. Нередко данному заболеванию сопутствуют многоводие, поражение почек, сердца, нервной системы. Выявить атрезию тонкой кишки с помощью УЗИ очень сложно, чаще всего она обнаруживается в середине беременности или на поздних сроках. Атрезия толстой кишки УЗ-диагностике не поддается. Из нарушений строения передней брюшной стенки в большинстве случаев выявляют омфалоцеле.
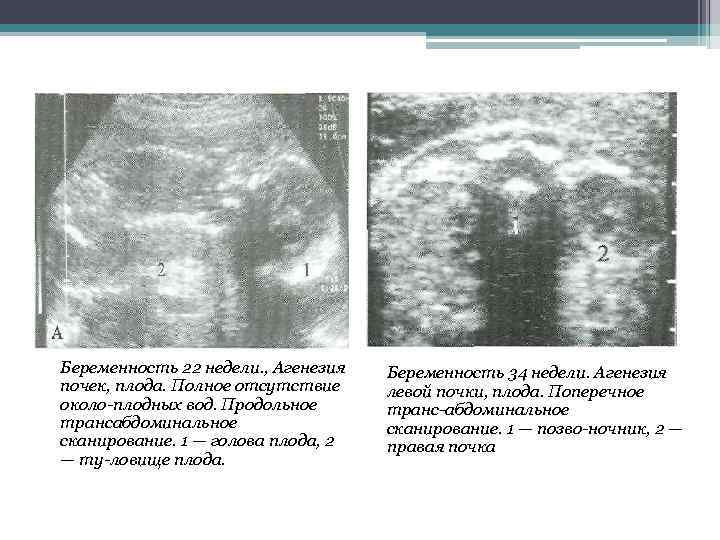
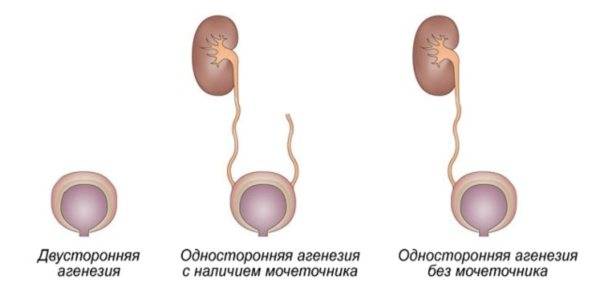
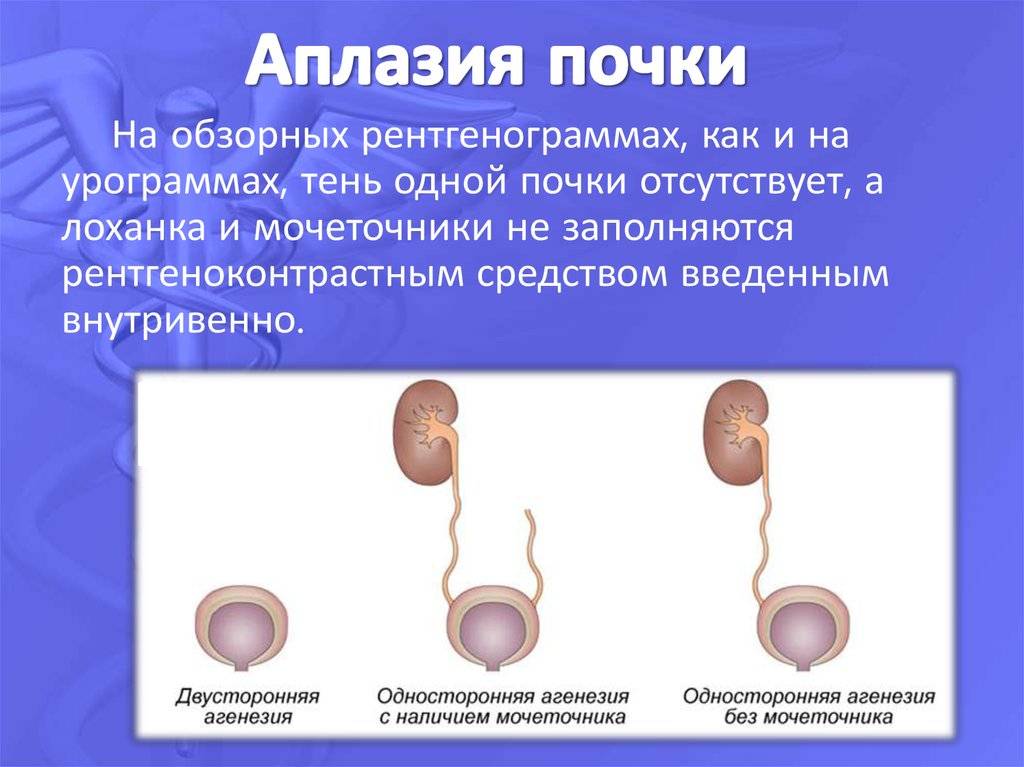
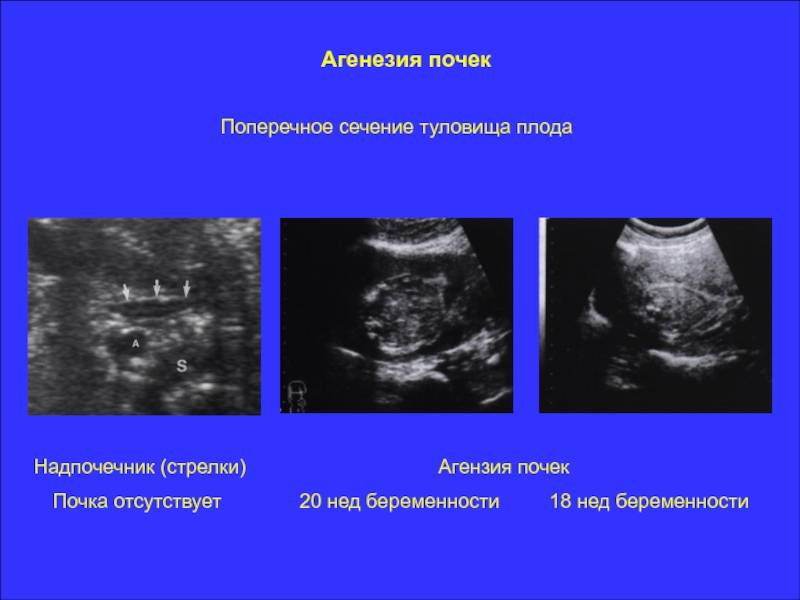
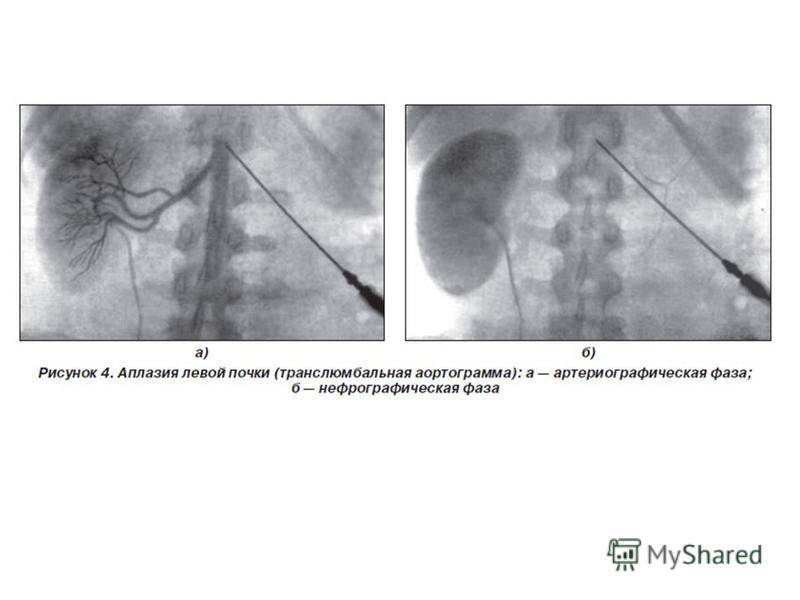
Некоторые из аномалий мочевыделительной системы приводят к очень страшным последствиям, поэтому если патология выявлена на ранних сроках, врач может посоветовать прерывание беременности. Если заболевание обнаружено поздно, меняют тактику ведения беременности. С помощью УЗИ можно обнаружить патологическую двустороннюю обструкцию, мультикистозную почку; диагностирование агенезии (отсутствия) органа бывает затруднено. Определение гидронефроза потребует повторного проведения УЗИ.
Асцит – свободная жидкость – на УЗИ видится как анэхогенная зона, которая окружает органы плода. Только после тщательного изучения результатов обследования ставится окончательный диагноз. На водянку указывают утолщение кожи либо наличие жидкости минимум в двух естественных полостях. К этому заболеванию приводят:
- врожденные сердечные пороки;
- резус-конфликт;
- обструкции лимфатических и кровеносных сосудов;
- аритмии.
Для точного диагностирования водянки пациентке назначают дополнительное экспертное УЗИ.
Многоводие также можно обнаружить с помощью УЗИ. Развитию данной аномалии способствуют:
- водянка плода;
- сахарный диабет (у матери);
- нарушения в формировании органов ЖКТ;
- патологии нервной трубки;
- многоплодная беременность;
- скелетные дисплазии грудной клетки;
- пороки строения передней стенки живота.
Маловодие провоцируют:
- двусторонняя аномалия почек;
- задержка внутриутробного развития;
- перенашивание беременности;
- повреждение амниотических оболочек;
- внутриутробная гибель плода.
Процедура УЗИ абсолютно безопасна для жизни и здоровья матери и ребенка, не имеет ограничений по количеству сеансов, поэтому не пренебрегайте рекомендациями доктора и своевременно проходите назначенное обследование.
Вся информация носит ознакомительный характер. Если у вас возникли проблемы со здоровьем, то необходима консультация специалиста.
Профилактика врожденных пороков
Профилактика врожденных пороков предусматривает проведение индивидуальных и массовых мероприятий. Индивидуальные методы профилактики врожденных пороков основаны на медико-генетическом консультировании, где специалист определяет степень риска развития врожденного порока плода. Чаще всего к генетику обращаются семьи, в которых есть наследственные или врожденные патологии у кого-либо из родственников. Для проведения оценки рисков развития врожденной патологии плода проводят методы пренатальной диагностики для определения состояния здоровья родителей. Часто составляют проектирование совокупности генов, позволяющее определить риск формирования врожденного порока развития плода из-за нарушений генетического материала или составления неправильных комбинаций. Помимо этого, для профилактики врожденных пороков будущим родителям следует вести правильный образ жизни и отказаться от вредных привычек.
К массовым методам профилактики врожденных пороков относятся:
- оздоровление окружающей среды;
- клинические испытания лекарственных препаратов, пищевых добавок и гербицидов на тератогенность;
- защита половой системы во время рентгенологического обследования;
- улучшение условий работы на вредных производствах;
- просвещение населения о врожденных пороках новорожденных.
Бесплатный прием репродуктолога
по 31 мая 2021Осталось дней: 32
Уважаемые пациенты! Клиника «Центр ЭКО» приглашает вас на бесплатный прием репродуктолога с проведением УЗИ и составлением плана лечения.
Другие статьи
Внимание! Важная информация о работе клиники
Уважаемые пациенты! Забота о вашем здоровье и безопасности – наш долг. «Центр ЭКО» предпринимает все необходимые меры для вашей защиты, в соответствии с рекомендациями Министерства Здравоохранения и Роспотребнадзора по предотвращению распространения вирусной инфекции.
Читать статью
Что такое ЭКО в естественном цикле
Протокол ЭКО в естественном цикле (ЕЦ) – наиболее щадящая процедура из всех программ экстракорпорального оплодотворения.
Читать статью
Приобретённые патологии плода
Приобретенные патологии возникают под воздействием негативных факторов (радиация, токсическое отравление) и образа жизни матери (алкоголизм, курение, наркомания).
Врождённые пороки органов и костей
Редко у плода развивается один такой порок, обычно это комплекс патологий, затрагивающих несколько жизненно важных органов.
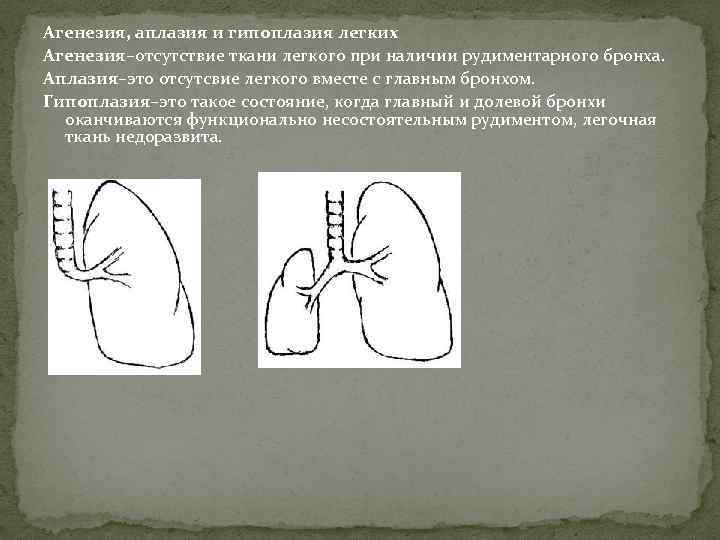
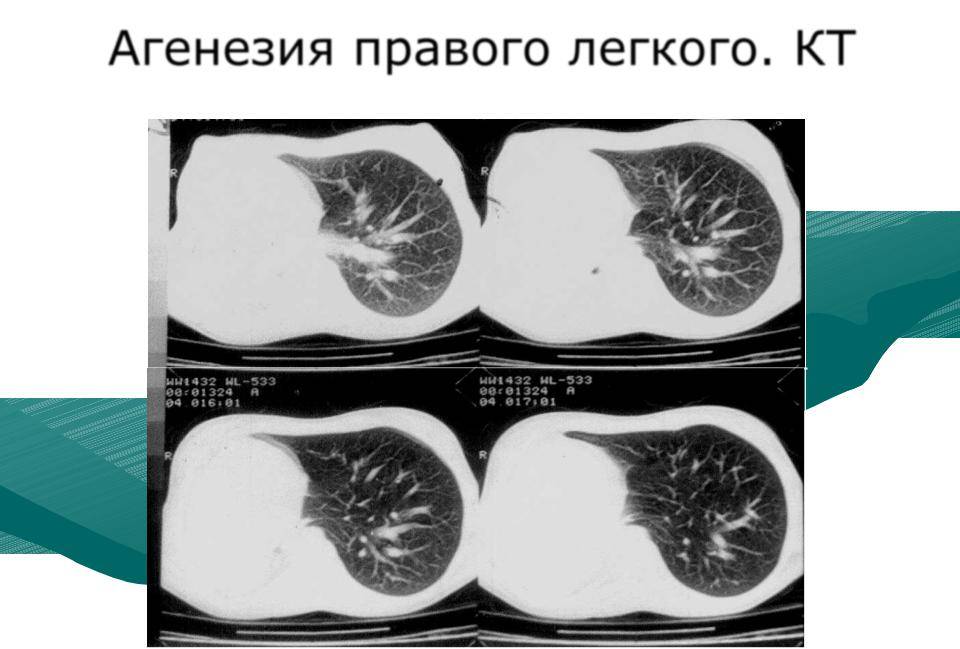
Врождённые пороки имеют следующие разновидности:
- аплазия — полное отсутствие органа с сохранением сосудистой ножки;
- агенезия — полное отсутствие органа без сохранения сосудистой ножки;
- гипоплазия — недоразвитость органа;
- дистопия — расположение органа в неположенном месте.
Ультразвуковая диагностика врождённых пороков проводится трижды:
- 1-я диагностика — 10-13 недель;
- 2-я диагностика — 19-20 недель;
- 3-я диагностика — 31-32 недели.
Исследование позволяет выявить большинство патологий:
- отсутствие или деформацию органа;
- анэнцефалию (отсутствие головного мозга);
- атрезию (отсутствие) конечностей;
- аномалия скелета лица (заячья губа, волчья пасть);
- незаращение спинномозгового канала;
- пороки сердца;
- гидроцефалия (скопление жидкости в головном мозге).
Гипертензионно-гидроцефальный синдром
Это патология, при которой спинномозговая жидкость скапливается под мозговыми оболочками. Осложнение выявляется на УЗИ на поздних этапах беременности.
Характеризуется большим объёмом головы плода, диспропорцией между мозговыми долями, выпиранием родничка. Чем раньше выявлена патология, тем больше шансов на благоприятный исход.
Гидроцефалия
Это скопление спинномозговой жидкости в желудочках головного мозга, в результате чего они увеличиваются в размерах, и возрастает внутричерепное давление.
Гидроцефалию выявляют на 2 семестре беременности. Главным показателем является увеличение высоты тела желудочка головного мозга выше нормы (свыше 1,1 см). При этом снижается эхогенность межполушарной щели при одновременном увеличении ширины щели свыше 5 мм.
Пороки сердца
Пороки сердца у плода — не редкость. На УЗИ они обнаруживаются на 2-м плановом осмотре (скрининговом УЗИ второго триместра).
К ним относятся:
- гипоплазия левой стороны сердца;
- отсутствие сообщения между правыми камерами сердца;
- отсутствие одного из желудочков сердца;
- патология сердечной мышцы;
- аритмия;
- брадикардия;
- сужение просвета аорты;
- сужение лёгочной артерии;
- порок трикуспидального клапана;
- тетрада Фалло (сочетанная аномалия сердца).
Большая часть сердечных патологий исправляется хирургическим путём. Чем раньше проведена операция, тем больше шансов на успешное выздоровление.
Врождённые патологии плода — трисомии
 Такие патологии встречаются часто, но большинство эмбрионов с хромосомными аномалиями гибнут внутриутробно в результате спонтанных выкидышей. Трисомии имеют генетическую природу и возникают в момент зачатия.
Такие патологии встречаются часто, но большинство эмбрионов с хромосомными аномалиями гибнут внутриутробно в результате спонтанных выкидышей. Трисомии имеют генетическую природу и возникают в момент зачатия.
Чтобы предупредить рождение малышей с тяжелыми патологиями, семейным парам, планирующим рождение ребёнка, рекомендуют пройти кариотипирование — изучение хромосомных наборов, позволяющее определить генетическую совместимость и возможность иметь здоровое потомство.
Кариотипирование имеет 99% достоверность, благодаря которой можно заранее узнать, имеют ли супруги предрасположенность к хромосомным мутациям.
На ранних сроках без специальных анализов обнаружить трисомию невозможно. С этой целью проводится перинатальный скрининг — серия анализов, определяющих врождённые аномалии плода. Первый скрининг проводится на сроке 11-13 недель и включает ультразвуковую диагностику и анализы крови на гормоны.
Скрининг проводится добровольно. Но процедуру настоятельно рекомендуется пройти женщинам из группы риска, которые:
- забеременели в возрасте старше 35 лет;
- имели замершие беременности;
- подвергались ионизированному или радиационному облучению;
- работают на предприятиях химической промышленности;
- имеют вредные привычки (курение, употребление алкоголя и наркотиков);
- неблагоприятная экологическая обстановка;
- возраст отца ребенка старше 50 лет.
УЗИ определяет:
- положение эмбриона в матке (исключение внематочной беременности);
- количество плодов (одноплодная или многоплодная беременность);
- форма конечностей, черепа, строение лица;
- сердцебиение;
- устанавливается копчико-теменной размер (высота плода от копчика до темечка);
- нормальное или патологическое строение головного мозга;
- толщина воротникового пространства:
- размер носовой кости:
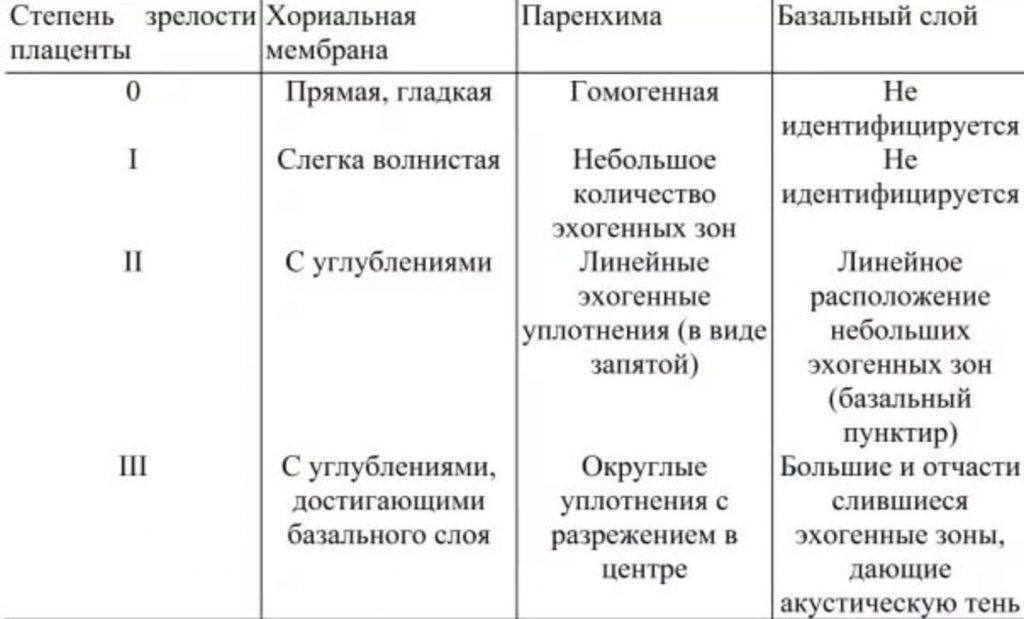
- зрелость и функциональность плаценты.